鼻咽癌是一种起源于鼻咽上皮的恶性肿瘤,在中国南方、东南亚、中东部分地区和北非属于高发癌症。尤其在我国南方的广东、广西、福建及香港地区,年发病人数可达 15 万。
而在另一方面,鼻咽癌起病隐蔽,确诊时,多数患者已处于局部晚期(III–IV 期)。一旦一线治疗失败,二线治疗方案的客观缓解率(ORR)仅有 20%,中位无进展生存期(PFS)就只剩下短短的 3~7 个月。
这类患者,还能否有新的治疗希望?
近日,中山大学肿瘤防治中心张力教授团队在 2025 年欧洲肿瘤学学会年会(ESMO)上公布了 BL-B01D1–303 研究的最新结果,为鼻咽癌的治疗提供了重要思路。
研究同期发表于《柳叶刀》。丁香园特邀 中山大学肿瘤防治中心张力教授 共同解读。

针对这类患者,首个 III 期临床来了
当前,针对复发/转移性鼻咽癌的一线标准治疗,是含铂化疗联合程序性死亡受体-1(PD-1)抑制剂。虽然该方案显著改善了疗效,但绝大多数患者最终仍会出现疾病进展。
一旦一线治疗失败,二线治疗方案的客观缓解率(ORR)只有 20%,中位无进展生存期(PFS)就只剩下短短的 3~7 个月。
而如果已经用过至少两种系统治疗方案(包括含铂化疗和 PD-1/PD-L1 抑制剂)后仍然进展的复发/转移性鼻咽癌患者,通常就只剩下挽救性化疗方案这一条路,ORR 低至 15% 以下,中位 PFS 仅为 2~4 个月。
本次,张力教授团队的最新研究是一项 III 期临床试验,探索双特异性药物偶联物 BL-B01D1 对于化疗和 PD-1/PD-L1 抑制剂治疗后进展的复发或转移性鼻咽癌患者的效果。
这也是首个针对既往接受过大量治疗的复发/转移性鼻咽癌患者的随机 III 期临床试验。

论文截图
超过 80% 的鼻咽癌肿瘤中不仅表达人表皮生长因子受体 3(HER3),还存在表皮生长因子受体(EGFR)过表达,且与不良预后相关。
作为靶向 EGFR 和 HER3 的 ADC 新星,BL-B01D1 已在临床前研究及早期临床试验(如 I 期研究 NCT05194982)均显示出积极的抗肿瘤活性和可控的安全性。
最新公布的 BL-B01D1-303(NCT06118333)是一项多中心、随机、开放标签的 III 期临床试验,在国内 55 家医院进行,研究纳入 18~75 岁、既往接受 ≥2 种一线系统治疗(必须含铂类方案和 PD-1/PD-L1 抑制剂),经组织学/细胞学确诊的复发/转移性鼻咽癌的患者(ECOG 评分 0~1 分,预期生存期 ≥12 周)。
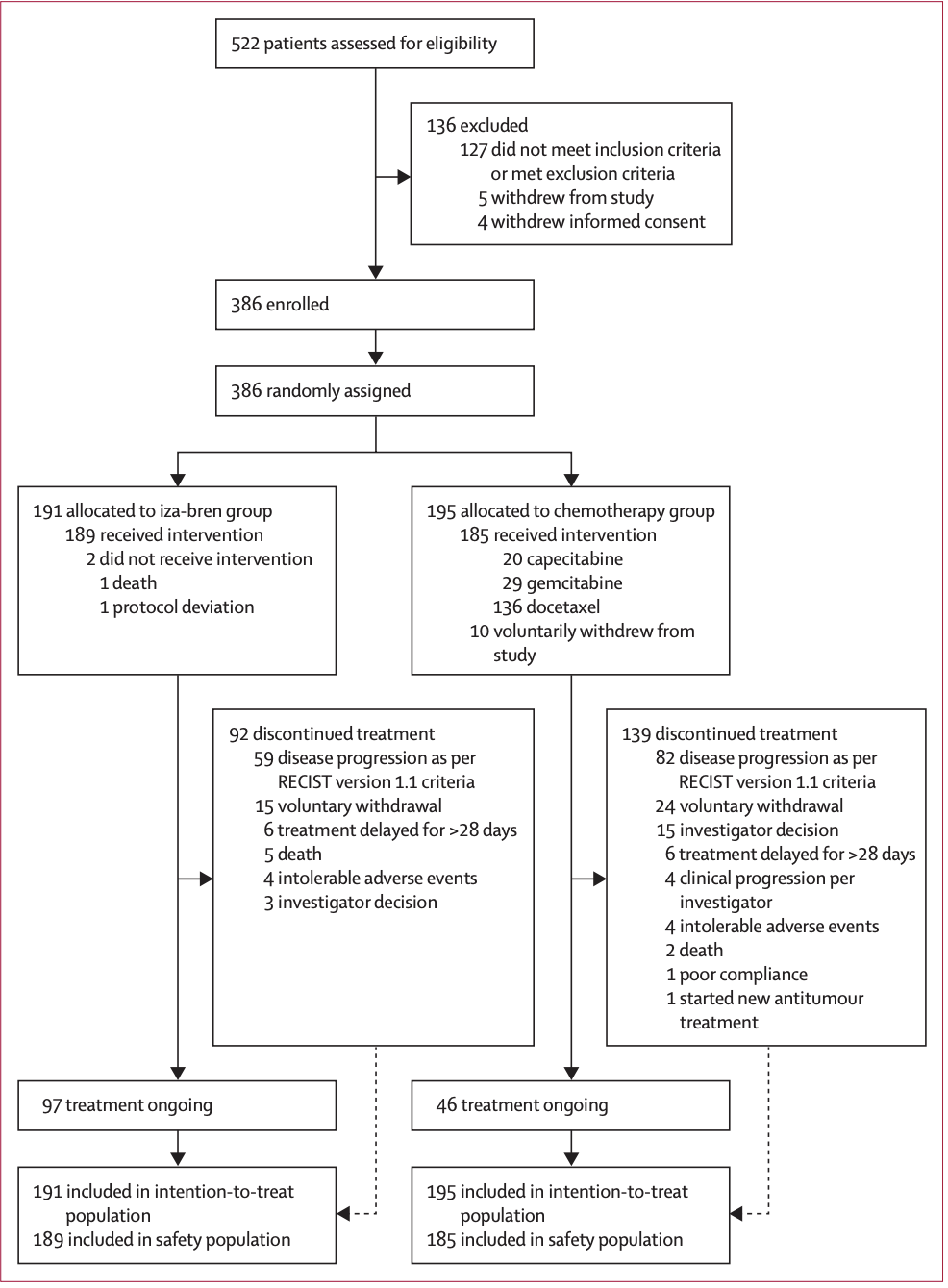
论文截图
实验组应用 BL-B01D1(2.5 mg/kg),第 1、8 天静脉输注,每 3 周为一个周期。对照组则由研究者根据患者实际情况评估,选择以下标准化疗方案中的一种:
卡培他滨(1000mg/m²,每日 2 次,d1-14,q3w)
吉西他滨(1000mg/m²,d1、8,q3w)
多西他赛(75mg/m²,q3w)
研究主要终点为独立盲法中心评估的客观缓解率(ORR)和总生存期(OS,当前研究阶段还不能报告该数据)。
研究结果显示,BL-B01D1 组 ORR 为 54.6% (95%CI 45.2-63.8%),比作为对照的化疗组高出 27.9%(p<0.0001)。 除了主要终点,其他数据表现也都十分亮眼。 BL-B01D1 组与化疗组相比,中位无进展生存期(PFS)为 8.38 个月(95%CI 6.37-9.92)vs 4.34 个月(95%CI 4.04-5.62);风险比(HR)为 0.44(95%CI 0.32-0.62);中位缓解持续时间(DoR)为 8.51 个月 (95%CI 6.97-NR)vs 4.76 个月(95%CI 4.04-6.93)。并且,以上疗效优势在全部预设亚组中均保持一致。
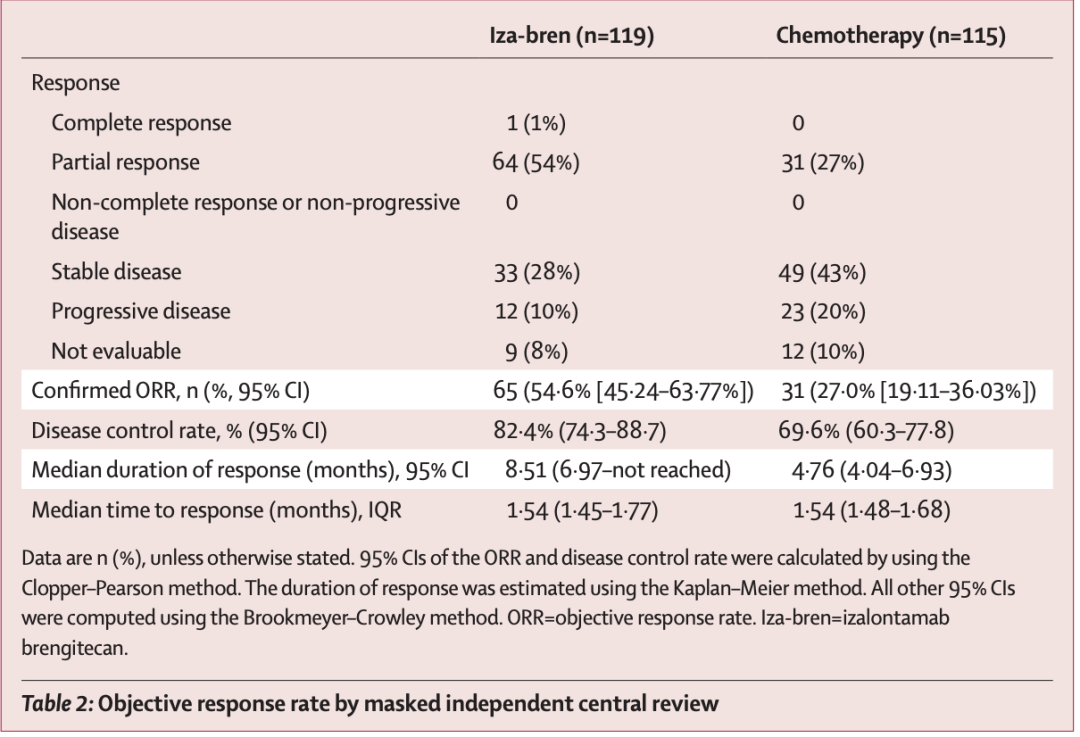
论文截图
全球潜在首款:84 亿美元出海,已纳入优先审评
来自百利天恒的 BL-B01D1 (BL-B01D1),也是一款近年来 ADC 领域的一款明星药。
2023 年 12 月,百利天恒与 BMS 达成合作,BL-B01D1 在中国由百利天恒独家开发,在中国以外的地区由西雅图免疫与百时美施贵宝共同开发,总金额高达 84 亿美元,其中首付款 8 亿美元。不仅创下国内创新药 license out 交易的首付款纪录,也刷新了当时全球 ADC 单药交易总价的纪录。

图源:百利天恒官网
据官方介绍,该药为我国自主研发、全球首创(First-in-class)、新概念(New concept)且唯一进入 III 期临床试验阶段的 EGFR×HER3 双抗 ADC。
截至本月,BL-B01D1 在中国和美国已开展了近 40 项针对多种肿瘤类型的临床试验,包括一线晚期三阴性乳腺癌的 II/III 期临床试验、EGFR-TKI 耐药后晚期非小细胞肺癌的 II/III 期临床试验和经治晚期转移性尿路上皮癌的II/III 期临床试验,以及非小细胞肺癌、晚期实体瘤等多项 I/II 期临床试验。
而本次公布的最新研究,聚焦于鼻咽癌这一难题。
「鼻咽癌是一个地域性的疾病,此前很长一段时间并不受到重视。」张力教授说,「对于患者来说,目前标准的一线治疗是化疗联合免疫治疗,但很容易出现耐药。而二线治疗缓解期都也很短,等到了三线,患者基本上就没有任何治标准治疗了。」
张力教授介绍,作为双抗 ADC,BL-B01D1 具有两大优势。
首先,相比于其他 ADC,BL-B01D1 的皮肤毒性更低。
由于 EGFR 在皮肤角质形成细胞中高度表达,传统 EGFR 单抗会导致皮疹、干燥、瘙痒等典型「皮肤毒性」症状。而 BL-B01D1 抗体部分的双特异结构经设计后,对同时表达 EGFR 和 HER3 的细胞结合亲和力最高。可以避免伤害「高表达 EGFR 但低表达 HER3」的皮肤上皮细胞,从而降低「皮肤毒性」。
另一方面,BL-B01D1 能够有效克服肿瘤抗原的异质性。
在传统 ADC 或单抗治疗中,常见的耐药机制之一就是抗原异质性表达:当治疗靶点(例如 EGFR)被药物长期抑制后,肿瘤细胞会通过内吞降解、突变或信号反馈调控等方式降低该受体的表达,导致单靶 ADC 效果下降。
EGFR 与 HER3 在多数上皮性肿瘤中常形成异源二聚体。当抑制 EGFR 时,肿瘤往往改走 HER3 通路,反之亦然。而 BL-B01D1 同时靶向两者,使得 EGFR/HER3 异源二聚体无法形成,降低了单一抗原下调带来的失靶风险。
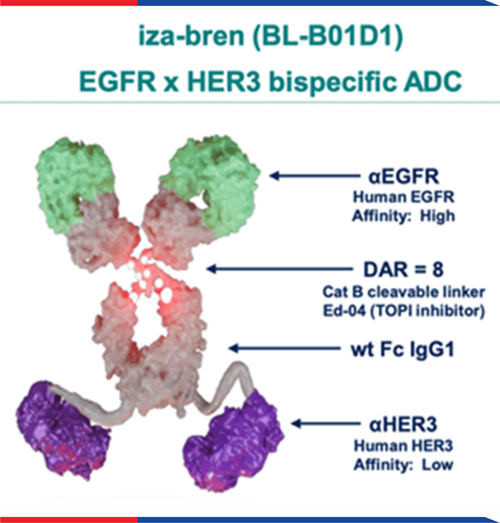
图源:参考资料
目前,BL-B01D1 已于 9 月正式纳入我国 CDE 优先审评,适应症为既往经治的复发性或转移性鼻咽癌。
「BL-B01D1 III 期试验的最终结果,还需要等待总生存期的随访数据。」张力教授说,「相信在不远的将来,BL-B01D1 将很快走上临床,不仅造福中国的患者,也给全球的患者带来新的希望。」
策划:z_popeye|监制:islay
